Comment les filaments d'actine s'organisent à l'intérieur des cellules et des tissus vivants
En utilisant la microscopie de fluorescence résolue en polarisation, les biologistes et physiciens de l'Institut Fresnel, associés à une équipe internationale, sont parvenus à générer des nouveaux outils moléculaires qui permettent d'observer l'organisation des filaments d'actine impliqués dans de nombreux processus cellulaires. Ces résultats sont publiés dans la revue Cell.
L'actine est une protéine qui joue un rôle clé dans de nombreux processus cruciaux pour la croissance et le fonctionnement des animaux, tels que la division et le déplacement des cellules, ou la contraction des muscles. Elle réalise ces différentes tâches en formant des filaments, qui s'organisent de manière spécifique pour accomplir les différentes fonctions. Pour visualiser les filaments d'actine dans les cellules, les biologistes utilisent la microscopie de fluorescence. Mais cette méthode ne donne pas d'informations sur la manière dont sont organisés les filaments. Une technique d'observation développée à l'Institut Fresnel (Aix-Marseille Université/Centrale Méditerranée/CNRS), la microscopie de fluorescence résolue en polarisation, permet de dépasser cette limite. Grâce au travail mené avec une équipe internationale1 de biochimistes, de biologistes structuraux et cellulaires et de biophysiciens, cette technique permet de déterminer l'organisation des filaments d'actine dans des cellules vivantes, c'est-à-dire leur orientation dans l'espace et leur alignement. Des données essentielles pour comprendre le lien entre l'organisation des filaments et les fonctions qu'ils accomplissent.
La microscopie de fluorescence utilise des protéines qui peuvent absorber la lumière d'une couleur et émettre une lumière d'une autre couleur. La plus connue est la GFP (Green Fluorescent Protein), qui brille en vert lorsqu'elle est exposée à la lumière bleue. En attachant ces protéines fluorescentes à l'actine à l'intérieur d'une cellule, les chercheurs sont en mesure de localiser les filaments d'actine, mais pas de savoir comment ils sont organisés. La microscopie de fluorescence résolue en polarisation, en revanche, en mesurant comment la fluorescence varie en fonction de la rotation de la polarisation de la lumière, fournit des informations sur l'orientation des protéines lumineuses, qui reflètent l'organisation des filaments d'actine auxquels elles sont liées... à condition d'être immobilisées par rapport au filament. C'est ce qu'ont réussi à faire les chercheurs, en utilisant des outils issus du génie génétique. Leur méthode consiste à créer une liaison entre un monomère d'actine, ou une protéine qui s'associe à l'actine, et une protéine fluorescente dont la mobilité est contrainte, en fusionnant les ADN de chacun : lorsque l'ADN fusionné est introduit dans une cellule, celle-ci fabrique directement ces protéines de fusion fluorescentes qui en s'associant aux filaments d'actine permettent de mesurer leur organisation par la microscopie de fluorescence résolue en polarisation. L'étude de l'organisation des filaments d'actine peut ainsi être réalisée dans toutes sortes de cellules animales. Le logiciel d'analyse de données (open source) PyPOLAR, co-développé avec l'Institut de mathématiques de Marseille (I2M, Aix-Marseille Université/CNRS), facilite l'interprétation des images par les biologistes.
Pour illustrer le large domaine d'utilisation de la méthode, des essais ont été réalisés avec des cellules de levure, de nématode (un petit ver), et des muscles de vol de la mouche drosophile. Les perspectives sont nombreuses, en particulier pour les biophysiciens qui étudie la mécano-biologie : les forces impliquées dans les processus cellulaires d'adhésion, de déformation, de migration, ou encore dans la morphogénèse d'organes ou d'embryons. À plus long terme, la méthode pourrait servir à des études de pathologies, par exemple sur la myopathie. L'observation de l'actine, aujourd'hui réalisée dans le plan, est en cours d'extension à la mise en évidence de l'organisation 3D des filaments.
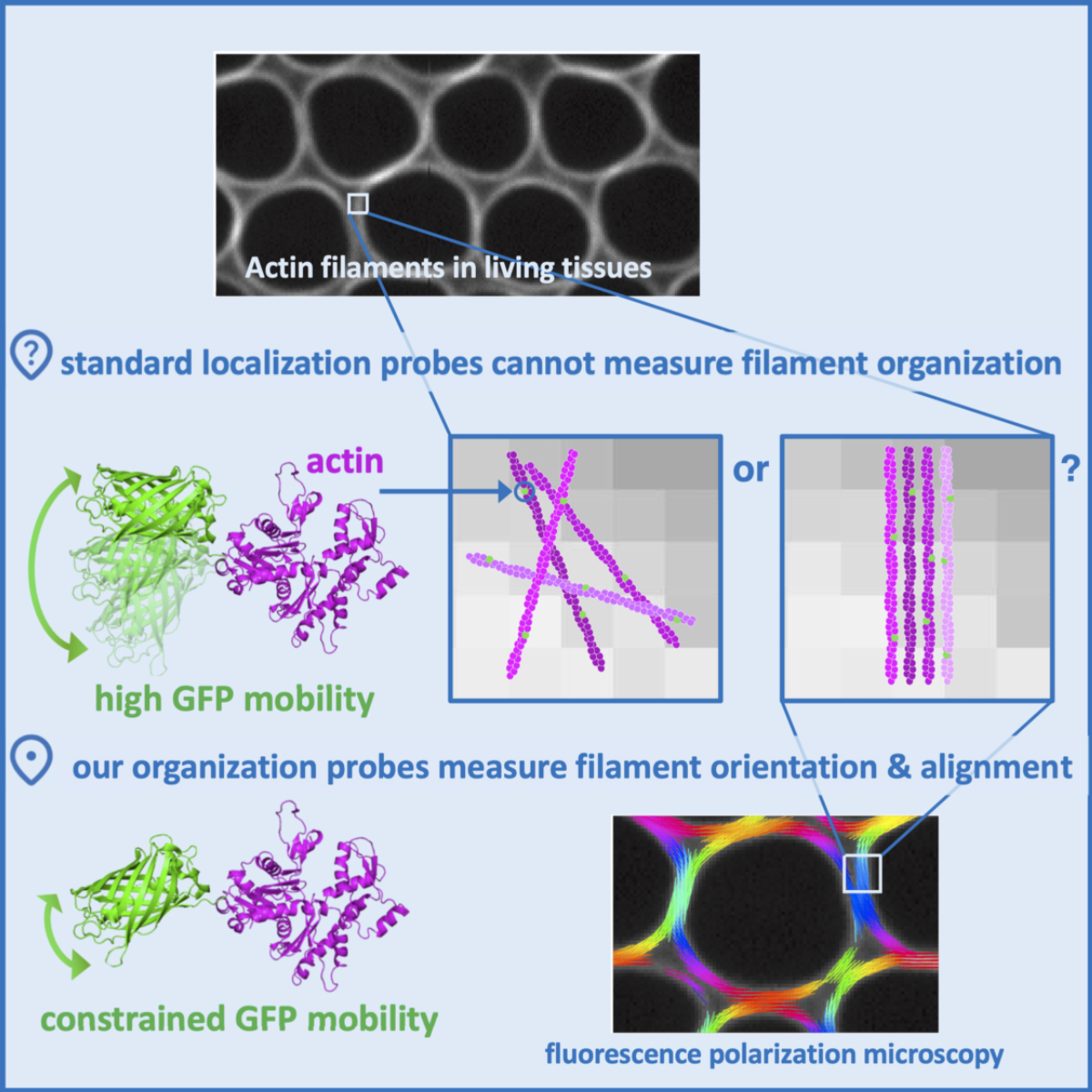
© Institut Fresnel
Reférences
Genetically encoded reporters of actin filament organization in living cells and tissues.
Carla Silva Martins, François Iv, Shashi Kumar Suman, Thomas C. Panagiotou, Clara Sidor, María Ruso-López, Camille N. Plancke, Shizue Omi, Rebecca Pagès, Maxime Gomes, Alexander Llewellyn, Sourish Reddy Bandi, Laurie Ramond, Federica Arbizzani, Caio Vaz Rimoli, Frank Schnorrer, François Robin, Andrew Wilde, Loïc LeGoff, Jean-Denis Pedelacq, Antoine Jégou, Stéphanie Cabantous, Sergio A. Rincon, Cristel Chandre, Sophie Brasselet, Manos Mavrakis.
Cell, publié le 1er mai 2025.
https://doi.org/10.1016/j.cell.2025.03.003
Article consultable sur les bases d’archives ouvertes HAL
- 1Cette recherche est le fruit d’une collaboration entre l’Institut Fresnel (Marseille, France), l’Institut de biologie Paris-Seine (IBPS, Paris, France), l’Université de Toronto (Canada), l’Institut de biologie du développement de Marseille (IBDM, Marseille, France), l’Instituto de Biología Funcional y Genómica and Departamento de Microbiología y Genética (IBFG, Salamanca, Espagne), l’Institut Jacques Monod (Paris, France), l’Institut de pharmacologie et de biologie structurale (IPBS, Toulouse, France), le Centre de recherche en cancérologie de Toulouse (CRCT, Toulouse, France) et l’Institut de mathématiques de Marseille (I2M, Marseille, France).
