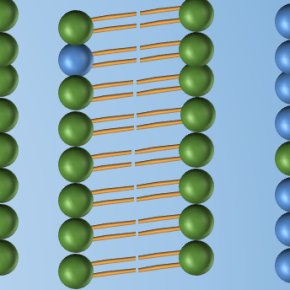
Quand l’évaporation trie les lipides
Une équipe de recherche franco-suédoise a montré que l’évaporation de l’eau peut provoquer la séparation spontanée de deux lipides pourtant très proches chimiquement. En créant un gradient d’hydratation, l’évaporation réorganise localement la composition du mélange, jusqu’à inverser les proportions initiales. Ces résultats sont publiés dans la revue PNAS.
Lorsqu’un mélange aqueux est exposé à l’air, l’évaporation crée un gradient d’hydratation : plus sec près de l’interface, plus hydraté en profondeur. De tels gradients existent dans certaines membranes biologiques exposées à l’air, mais aussi dans de nombreux procédés de séchage de revêtements ou de films fonctionnels. Les chercheurs ont étudié un mélange de deux phospholipides très proches : le DPPC, qui forme une phase lamellaire rigide, et le DOPC, qui forme une phase lamellaire fluide. Ces molécules ne diffèrent que par la présence de doubles liaisons dans leurs chaînes carbonées.
Grâce à une combinaison de microscopie Raman confocale et de diffusion des rayons X (SAXS/WAXS), des scientifiques du Laboratoire de génie chimique (LGC, CNRS/Toulouse INP/Université de Toulouse) et de l’Université de Lund (Suède) ont cartographié simultanément la teneur en eau, la composition et l’organisation des structures auto-assemblées le long du gradient.
Résultat : les lipides ségrèguent spontanément dans le gradient d’hydratation.
Le DPPC s’accumule dans la zone la plus sèche, près de l’interface air/liquide, tandis que le DOPC migre vers une région intermédiaire plus hydratée. La composition locale peut même s’inverser par rapport au mélange initial.
Le mécanisme repose sur une différence structurale : les phases lamellaires formées par chacun des lipides n’incorporent pas la même quantité d’eau. La phase rigide associée au DPPC tolère peu d’eau, alors que la phase fluide associée au DOPC peut en accueillir davantage. Sous gradient d’hydratation, il devient donc favorable que chaque phase occupe la zone correspondant à sa capacité de gonflement. Bien que le système soit globalement hors équilibre, la ségrégation peut être décrite comme une succession d’équilibres locaux : les flux induits par l’évaporation s’organisent de manière à réduire l’énergie libre le long du gradient.
Ce travail met en évidence un principe général : dès que des composants diffèrent par leur affinité pour l’eau — ici à travers les structures qu’ils forment — un gradient d’hydratation peut induire une organisation spatiale marquée. Ces résultats ouvrent des perspectives pour la compréhension des membranes biologiques exposées à l’air (peau, poumon, film lacrymal), mais aussi pour la conception de revêtements fonctionnels, de systèmes de délivrance de médicaments ou de matériaux adaptatifs soumis à des variations d’humidité.
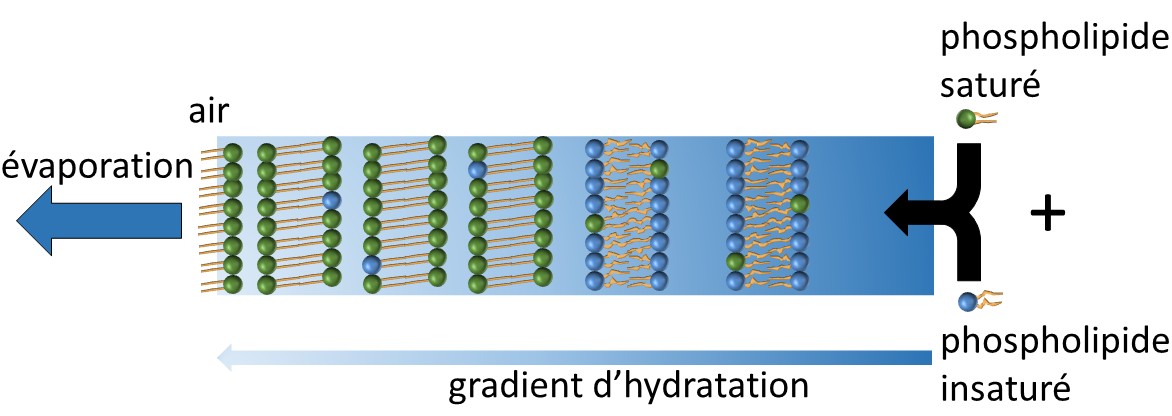
© Kevin Roger
Références
Hydration gradients drive lipid self-segregation.
Nikol Labecka, Jenny Andersson, E. Sparr, K. Roger.
PNAS, 06 février 2026.
https://doi.org/10.1073/pnas.2518553123